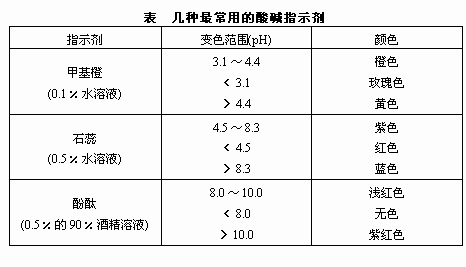
酸碱指示剂一般都是结构比较复杂的有机染料,它们本身是极弱的有机酸或有机碱,或是既表现为弱酸又表现为弱碱的两性物质。它们的分子和电离出的离子,由于结构不同而显不同的颜色。在溶液中分子与离子间保持平衡。当溶液pH改变时,平衡发生移动而引起颜色的变化。
例如:酚酞为一有机弱酸,用通式HIn代表,它未电离的分子HIn为无色,电离生成的阴离子In-为红色。在水溶液中存在着下列电离平衡:
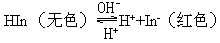
在酸性溶液中,平衡向左移动,
HIn浓度增加,溶液显无色。在碱性溶液中,H+与OH-结合成水,平衡就向右移动,In-浓度增大,溶液显红色。
根据质量作用定律,达到平衡时,
HIn分子与H+和In-离子的浓度之间有如下关系:

K
HIn是指示剂的电离常数,简称指示剂常数。它决定于指示剂的本性,在定温下是定值。酚酞指示剂的颜色是由In-与未电离的HIn的相对量决定的,其浓度比与KHIn和[H+]两因素有关。由于在定温下KHIn是定值,

比值的变化,从而影响指示剂的颜色。


微小变化,因而指示剂的颜色也随着发生很小的改变,但肉眼并不那么敏锐,察觉不出。一般地说,当
[In-]=10[HIn]时,人眼便只看到In-的颜色,当[HIn]=10[In-]时,只看到HIn的颜色。在这两个比值之间,看到的是逐渐变化的中间色,这就是指示剂的变色范围。
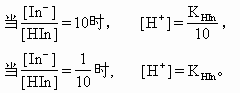
各取负对数:
pH=-lgKHIn±1,即pH=pKHIn±1。因此,pH=pKHIn±1,就是指示剂变色的pH范围。一般地说,指示剂变色的pH范围在pKHIn左右各1个pH单位,但由于人眼对不同颜色的敏感程度有差异,因此变色范围在pKHIn左右可略大于或略小于1个pH单位。例如酚酞(pK=9.1)的红色在无色中很易察觉,而无色在红色中较难察觉,因此它的变色范围在pK大的一面比较小些,而在pK小的一面反而大些,其变化范围是pH=8.0~10.0。pH<8为无色,pH>10为红色。
不同指示剂各有它的变色范围,在教科书或化学手册上可以查到。
将指示剂滴入被测溶液中,从指示剂显示的颜色便可判断溶液的
pH范围。例如,一溶液滴入酚酞时为无色,滴入甲基橙时显黄色,则这溶液的pH在4.4~8.0之间。除使用指示剂溶液外,还常把指示剂溶液浸透在滤纸条上,晾干后制成pH试纸。例如常用的石蕊试纸能粗略地测出溶液是酸性还是碱性。若要较精确地测出溶液的pH,可使用由多种指示剂混合液浸制成的试纸,例如“广泛pH试纸”,在pH0~14的范围内,不同pH时试纸显示不同颜色,预先制成标准色版,将试纸接触被测溶液后显示的颜色与标准色版比较:就可以知道溶液的pH。