|

一、金属的化学性质
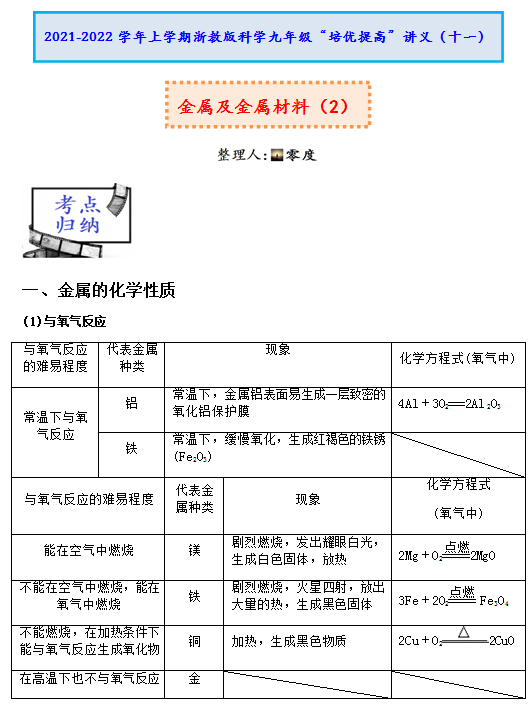
(1)与氧气反应
|
与氧气反应的难易程度 |
代表金属种类 |
现象 |
化学方程式(氧气中) |
|
常温下与氧气反应 |
铝 |
常温下,金属铝表面易生成一层致密的氧化铝保护膜 |
4Al+3O2===2Al 2O3 |
|
铁 |
常温下,缓慢氧化,生成红褐色的铁锈(Fe2O3) |
|
|
与氧气反应的难易程度 |
代表金属种类 |
现象 |
化学方程式
(氧气中) |
|
能在空气中燃烧 |
镁 |
剧烈燃烧,发出耀眼白光,生成白色固体,放热 |
2Mg+O2点燃2MgO |
|
不能在空气中燃烧,能在氧气中燃烧 |
铁 |
剧烈燃烧,火星四射,放出大量的热,生成黑色固体 |
3Fe+2O2点燃 Fe3O4 |
|
不能燃烧,在加热条件下能与氧气反应生成氧化物 |
铜 |
加热,生成黑色物质 |
2Cu+O2 2CuO 2CuO |
|
在高温下也不与氧气反应 |
金 |
|
|
(2)与酸反应:金属活动性顺序排在H前面的金属单质能与酸发生反应,生成相应的盐和氢气。相同条件下,金属与酸反应的剧烈程度也因金属活动性的强弱而不同,金属活动性越强,反应越剧烈。
|
金属 |
与盐酸反应 |
与稀硫酸反应 |
反应现象 |
|
镁 |
Mg+2HCl===MgCl2+H2↑ |
Mg+H2SO4===MgSO4+H2↑ |
剧烈反应,产生大量气泡,溶液仍为无色,生成的气体在空气中燃烧产生淡蓝色火焰 |
|
铝 |
2Al+6HCl===2AlCl3+3H2↑ |
2Al+3H2SO4===Al2(SO4)3+3H2↑ |
|
锌 |
Zn+2HCl===ZnCl2+H2↑ |
Zn+H2SO4===ZnSO4+H2↑ |
反应比较剧烈,产生大量气泡,溶液为无色,生成的气体在空气中燃烧产生淡蓝色火焰 |
|
铁 |
Fe+2HCl===FeCl2+H2↑ |
Fe+H2SO4===FeSO4+H2↑ |
反应缓慢,产生气泡,溶液由无色逐渐变为浅绿色,生成的气体在空气中燃烧产生淡蓝色火焰 |
|
铜 |
不反应 |
不反应 |
无 |
① 铁与酸发生置换反应,生成铁的化合物中铁元素的化合价为+2价,故溶液呈浅绿色。
② 金属与酸反应的剧烈程度不止与金属的活动性强弱有关,还与其他很多因素有关,如酸的浓度、金属与酸接触面积的大小、反应温度等。故在探究金属与酸反应快慢的问题时,一定要注意控制好变量。
③ 由于金属锌与稀硫酸的反应速率适中,便于对氢气进行收集,实验室常用锌与稀硫酸的反应来制取氢气;金属镁和铝与稀硫酸的反应速率过快,铁与稀硫酸的反应速率过慢,都不利于氢气的收集;浓盐酸具有挥发性,用盐酸制取的氢气中因含有氯化氢气体而不纯净,故不选择盐酸作为实验室制取氢气的原料。 |